
人类视觉皮层中的“失衡对话”:解码弱视的秘密
一只眼睛总也看不清,真的是眼睛的问题吗? 科学家最新研究发现,这种被称为弱视的情况,其实是大脑视觉回路在"掉链子"--来自弱视眼的信号在大脑中变弱了、传递得慢半拍。研究团队利用7特斯拉(7T)超高场功能磁共振成像(fMRI)和频率标记脑电图(EEG)技术,精细观察到了弱视者视觉皮层的信号变化。这些发现为我们理解弱视背后的神经机制提供了新视角,也为未来制定更有针对性的弱视治疗方案带来了希望。
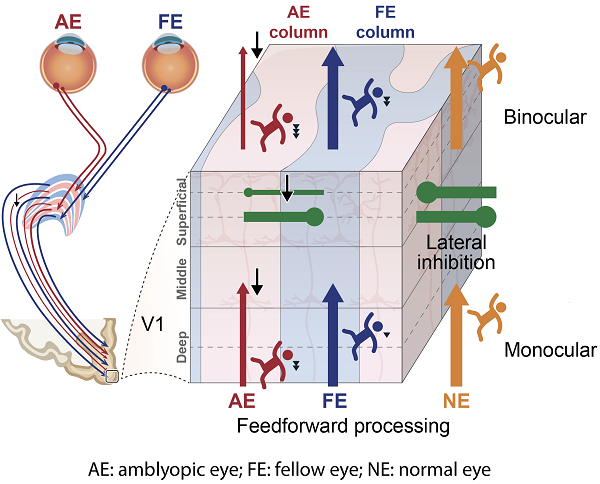
图1. 研究结果的总结示意图:弱视眼信号在传入皮层时已经受损,双眼互相抑制失衡、整合减弱,信号延迟增加。
弱视是什么?大脑让眼睛变"差"的常见视觉发育障碍
弱视(amblyopia)是一种常见的视觉发育障碍。它通常表现为一只眼睛的视力下降,即使配戴合适的眼镜矫正了眼球本身的屈光问题,视力仍达不到正常水平。我国约有1%-2%的儿童受到弱视影响,是儿童单眼视力损伤的首要原因。弱视常由幼年时期视觉输入异常引起,例如两眼屈光度差异过大(屈光参差)或斜视等,导致大脑在视觉发育关键期忽视了"差眼"的输入。久而久之,大脑更依赖于"好眼",而"差眼"的视觉功能发育受损。值得注意的是,弱视并非眼球结构的问题,而是大脑"看"的能力出了差错。因此,弱视为神经科学提供了一个研究早期经验如何塑造大脑可塑性的理想模型。
传统弱视治疗往往通过遮盖"好眼"来强迫大脑使用"差眼",但成年后弱视往往难以治愈,这提示大脑中某些回路可能在童年错过关键发育期后已经固化。然而,弱视的大脑机制长期不清楚--究竟大脑哪些环节"掉链子",才使得视力无法正常?这一谜题一直困扰着研究人员。最新的研究尝试解答这个问题,通过先进的脑成像技术窥探弱视者大脑视觉处理的细节。
7T fMRI和频率标记EEG:探查大脑活动的两大法宝
研究团队借助了两大技术"法宝":7特斯拉高分辨率功能磁共振成像(7T fMRI)和频率标记脑电图(EEG)。特斯拉是磁通量密度的单位,1特斯拉相当于地球磁场的约20000倍。fMRI扫描仪就像一台给大脑活动拍照的特殊相机,更高的场强相当于相机拥有更大的镜头,可以提供更精细的空间分辨率。7T fMRI拥有超高的场强,这意味着研究者能够分别观察大脑视觉皮层不同"层"的信号变化,这对于研究弱视非常关键--因为视觉皮层内不同层的神经元各司其职,可能有人专门"传话"、有人负责"处理"和"协调"。过去技术限制下,我们无法非侵入地看到如此精细的层级信息,7T fMRI的出现让这一切成为可能。
另一项技术频率标记EEG则发挥了时间分辨率高的优势。研究中,科学家让弱视受试者同时用两眼观看略有差别的视觉刺激,并给左右眼的刺激分别设置不同闪烁频率(比如左眼7.2 Hz,右眼8 Hz)。这样,大脑响应"差眼"和"好眼"的信号在EEG频谱上就会显示出对应的标签频率。通过分析脑电信号中不同频率成分的强度,研究者可以分别观察来自两只眼睛的反应强度,以及两眼信号在大脑中整合或相互抑制的情况。例如,如果双眼信号在大脑内结合,会出现两种频率相加产生的新频率成分;反之,若一只眼严重压制了另一只眼,则被压制眼的频率信号就会减弱。这种巧妙的频率标记方法,让研究团队如同给两只眼睛配上了不同色彩的墨水,能够同时追踪它们在大脑中的动态过程。
通过结合7T fMRI的高空间分辨率和频率标记EEG的高时间分辨率,研究者获得了前所未有的视角:既能看清弱视大脑中哪个"部位"、"哪一层"出了问题,又能精确测量出信号传递的时序变化。这为解析弱视的神经机制提供了有力工具。
大脑视觉皮层的"楼层"结构:分工明确,各尽其责
要理解这项研究发现,我们需要先认识大脑视觉皮层(尤其是视觉信号达到大脑皮层的第一站:初级视觉皮层V1)的分层结构。可以把V1想象成一栋六层的大楼:每一"层"神经元都有不同职责。其中,"中层"(大致对应V1的4C层)是信号输入层,相当于大楼的接待处--来自视网膜的视觉信息经由丘脑的中继站(外侧膝状体,LGN)在此层投递。当我们用眼睛看东西,这一层的神经元最先收到来自对应眼睛的原始图像信号。
"大楼"的上层(表层,V1第1/2/3层)既像一个会议室,也负责将信息传递到更高级的脑区。这里的神经元负责将来自左右眼的信号进行交流和整合。这些表层神经元横向连接丰富,在左右眼对应区域之间形成侧抑制和交互。打个比方,上层就像两个团队在开会,如果一只眼传来的信号过强,上层的侧抑制机制会让另一只眼的"声音"更小一些,反之亦然。如果这种抑制失衡,就会出现"一家独大"的局面。
而下层(深层,V1第5/6层)则更多负责向更低级的脑区传递反馈信息。可以说,中层拿信号、上层管整合和前馈、下层做反馈,各层联合作业,才能让我们两眼协作,获得清晰立体的视觉。
弱视眼信号减弱且延迟,双眼"拉锯战"失衡
那么,弱视究竟如何影响了上述"大楼"里的信息传递?研究结果揭示了三个关键问题:
◆ 弱视眼的信号"先天不足":7T fMRI显示,在弱视者的大脑中,来自弱视眼(简称AE)的视觉信号在进入V1的中间层时就已经显著减弱。就好比快递包裹一开始送到大楼接待处时,弱视眼这边的包裹又少又小。这种单眼信号的损失并非仅局限于V1:研究发现,向上传递到下游更高级的视觉区域(如V2、V3、V4)的过程中,这种差距一直存在。也就是说,弱视眼输入减弱导致了整个视觉通路链条上后续处理的"底子薄",这是视觉前馈信号受损的体现。
◆ 双眼互相抑制失衡、整合减弱:当同时给予双眼刺激时,V1表层的活动模式出现异常。正常情况下,两眼信号在表层应当相互平衡整合。但在弱视者中,研究观察到表层对弱视眼信号的响应下降更为明显。同时,强势的那只眼(好眼,FE)对"差眼"施加了强大的侧抑制,反过来弱视眼对好眼的抑制作用却相对减弱。两只眼睛在大脑中的"拉锯战"中,弱视眼完全落了下风,强眼一路压制,弱眼却无力反击,导致双方信息整合能力降低。脑电信号也显示代表双眼整合的频率成分(7.2 + 8 = 15.2 Hz)在弱视者中显著下降。这就解释了为什么弱视患者即使双眼同时睁开,大脑也很难将两只眼看到的影像融合为统一的立体画面--因为大脑里的整合机制出了问题,一只眼"声音太大"而另一只被"噤声"。
◆ 视觉信号处理速度变慢:研究还发现弱视会拖慢大脑处理视觉信息的节奏。通过频率标记EEG捕捉到的信号相位,研究者测量了大脑对刺激的响应时延,结果显示弱视眼引发的大脑反应相比正常情况有所延迟。不仅如此,在双眼共同刺激条件下,大脑整合两眼信息的整体速度也比正常人慢。对于弱视患者来说,大脑处理视觉的"内在时钟"被放慢了,效率降低,这可能进一步影响视知觉体验。
综上,图1形象地总结了弱视在大脑皮层各“楼层”造成的连锁影响:起始阶段,来自弱视眼的信号在V1输入层就衰减且滞后;随后,在表层与好眼信号交汇时出现不对称抑制,双眼融合受损;结果,整个视觉通路的信号强度和处理速度都降低。换言之,弱视的眼睛并非真的"差",而是它的信号一路上都在被"弱化"和"拖延"。这项研究精确定位了弱视这种视觉障碍在人类大脑神经环路中的对应改变。
为什么重要?大脑可塑性的启示与弱视治疗新希望
这些发现意义重大。首先,它回答了一个长期悬而未决的问题:弱视的神经损伤究竟源自何处?研究显示,问题的源头在于V1的输入层(接收来自丘脑的信号)发生了功能减弱和延迟。以往我们并不清楚弱视的缺陷主要是前馈信号不足还是高层反馈异常,现在证据倾向于前者--高层问题很可能是由底层信号不足继发的。明确了这一点,意味着未来治疗弱视需要抓住根源,比如设法增强弱视眼在低层次视觉通路中的输入和传递。这也印证了一个大脑可塑性的道理:幼年时期异常视觉经历会深刻地改变低阶神经回路的发展,如果错过关键期,成年后这些回路很难自发恢复。
其次,研究揭示的双眼整合与抑制失衡为弱视治疗提供了新思路。传统疗法侧重单眼视觉训练(如遮盖好眼练差眼),但近年来科学家意识到双眼训练的重要性,例如利用虚拟现实或双目分视训练游戏,来重新平衡大脑中两眼信号的关系。这项研究用脑成像直接证实了弱视者存在显著的双眼功能障碍,支持了同时训练两眼协作的策略。
最后,先进技术的应用本身就是一大进步。7T fMRI和频率标记EEG的结合,证明了我们有能力非侵入地窥测人脑内微环路级别的异常,这对不止弱视,对其他脑功能障碍的研究也具有借鉴意义。通过在毫秒级时间和亚毫米级空间上解析大脑活动,这类方法将帮助科学家更精细地绘制大脑功能图谱,理解不同疾病的机制差异。
展望:从科学发现走向临床应用
这项研究不仅让我们看清了弱视大脑皮层中"信号变弱变慢"的全过程,也为未来的干预指明了方向。了解了大脑哪个"楼层"出了问题,我们就有机会开发更有针对性的治疗手段--比如设计特定的视觉刺激程序来强化V1的输入层响应,或者利用脑刺激技术调节皮层层间的抑制平衡。令人振奋的是,同一团队的另一项研究已经展示出通过改良的增强现实训练可以提高弱视成年患者的双眼视觉机能:经过特殊视觉训练后,弱视眼的视力、眼优势及立体视功能均取得显著进步。这表明,即便成年后,大脑仍然保有一定的可塑性,可以通过训练部分逆转弱视带来的功能损伤。
展望未来,结合药物、视觉训练和新型脑机接口的综合干预可能进一步挖掘成年大脑的可塑性,让那些错过童年黄金期的弱视患者重新受益。正如研究者所强调的那样,只有弄清"大脑视界"里的细节,我们才能真正战胜弱视。
中国科学院生物物理研究所王跃博士、钱晨灿副研究员、高弋戈博士和复旦大学附属眼耳鼻喉科医院周钰莲眼科医师为论文共同第一作者,中国科学院生物物理研究所张朋研究员、钱晨灿副研究员、复旦大学附属眼耳鼻喉科医院文雯副主任医师为论文共同通讯作者,浙江大学电气工程学院张孝通长聘副教授为论文共同作者。该研究得到了科技创新2030-"脑科学与类脑研究"重大项目、国家自然科学基金、中国科学院青年创新促进会、温州医科大学眼视光学和视觉科学国家重点实验室项目、上海市科技创新行动计划专项资金的支持。
文章链接:https://doi.org/10.1162/imag_a_00561
附件下载: